
发布时间: 2025-10-29 09:51:11
2024年7月30日,在《Drug design,development and therapy》上发表一篇名为“Ceftazidime-Avibactam as a Salvage Treatment for Severely Infected Immunosuppressed Children”的研究论文,本研究旨在评估头孢他啶-阿维巴坦(CAZ/AVI)作为严重感染免疫抑制儿童的挽救治疗的疗效和安全性。
一、研究背景
头孢他啶-阿维巴坦(CAZ/AVI)是第三代头孢菌素头孢他啶和β-内酰胺酶抑制剂阿维巴坦的新型组合,对许多表达Ambler A类、C类酶、一些D类酶和许多耐药铜绿假单胞菌(PA)分离株表现出高体外活性,但不具有携带B类金属β-内酰胺酶的革兰氏阴性菌(GNB)。CAZ/AVI的上市后经验也被证明是治疗成人碳青霉烯类耐药肠杆菌科细菌(CRE)和其他耐多重耐药革兰氏阴性菌(MDR-GNB)感染的宝贵选择。几项针对患有血液系统疾病和器官移植的成人病例研究也证明了CAZ/AVI对MDR-GNB感染的疗效。然而,一些临床结果并没有为其使用提供足够的支持。儿科人群对CAZ/AVI的经验很少。只有两个患有血液系统疾病和肝移植的儿科患者病例系列显示CAZ/AVI成功治疗MDR-GNB和CRE感染。更多案例的积累将有助于改善CAZ/AVI的使用体验。同时,许多危重和免疫抑制儿童无法获得阳性GNB培养,尚不清楚CAZ/AVI是否是一种有效且安全的经验挽救选择。最近一项关于CAZ/AVI治疗成人血液癌患者MDR-GNB感染的综述也呼吁进行更多研究,以评估CAZ/AVI在这一弱势群体中的经验应用。
二、数据来源
这是一项单中心回顾性病例系列研究。纳入2019年9月至2022年7月期间接受CAZ/AVI至少48小时的患者。纳入标准为:(1)年龄<18岁;(2)治疗CAZ/AVI至少48小时。排除标准为:(1)接受CAZ/AVI治疗少于48小时的患者;(2)因违背建议而未能继续CAZ/AVI治疗;(3)当商业化抗菌药物敏感性测试存在不敏感性证据时,不恰当地开出CAZ/AVI。根据电子病历收集这些患者的临床信息。
三、研究方法
采用描述性统计总结患者特征。连续数据表示为标准差±平均值或中位数和四分位数范围,并根据数据分布是正态还是非正态,采用独立t检验或Wilcoxon秩和检验比较连续变量。分类变量以数字和百分比表示。Fisher精确检验(双尾检验)用于比较分类变量。对于病例匹配对,使用Wilcoxon符号秩和McNemar检验来比较特征和结果的差异。P值< 0.05被认为具有统计学意义。
四、主要结果
1.微生物学结果
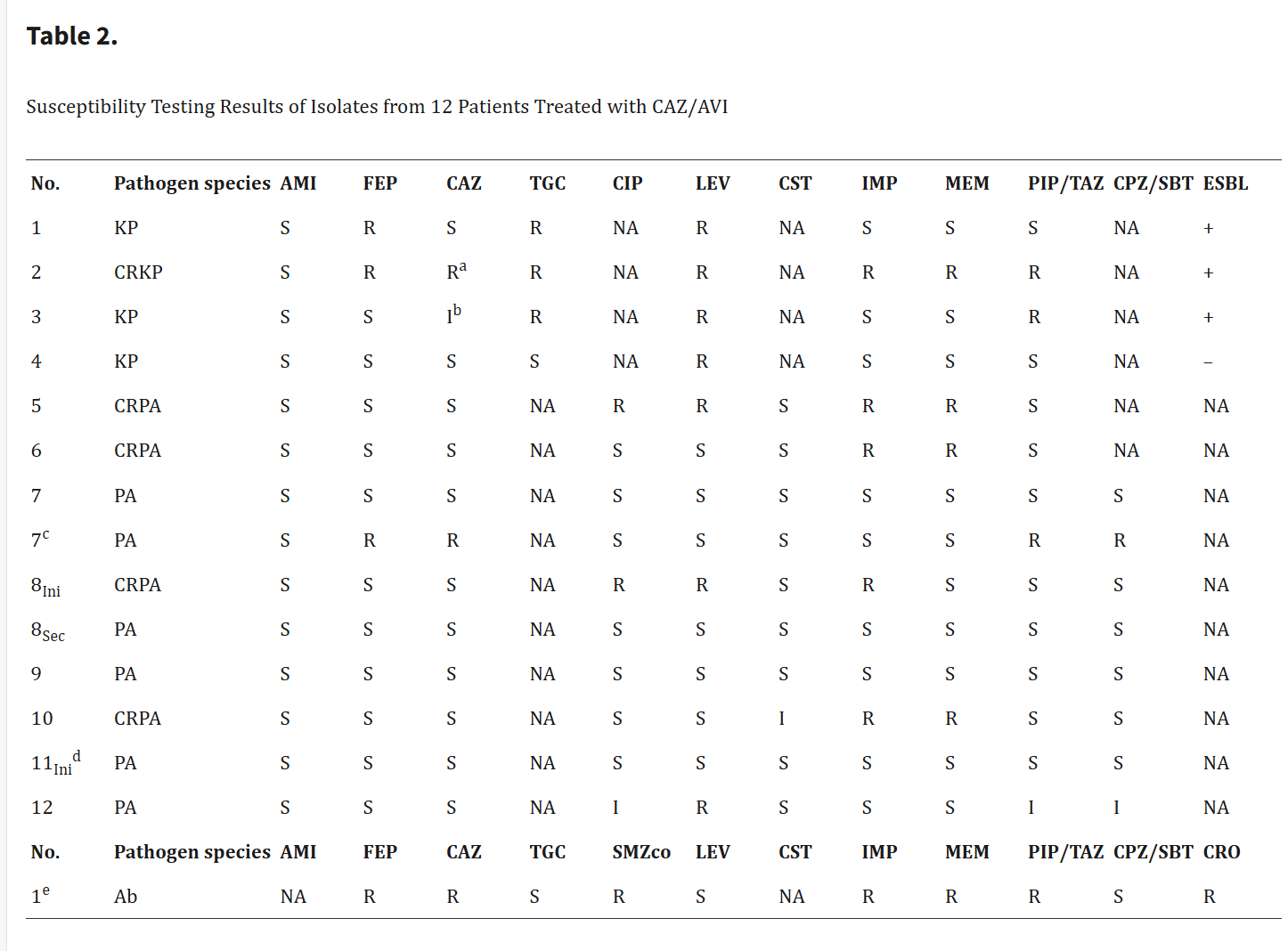
25例患者中有12例(48.0%)确诊GNB感染。表2共列出了15种分离株。肺炎克雷伯菌(KP)感染共4个病程,耐碳青霉烯类肺炎克雷伯菌(CRKP)1例,碳青霉烯类敏感KP(CSKP)3例。PA感染发生在9个病程中,其中4个耐碳青霉烯类铜绿假单胞菌(CRPA)和6个碳青霉烯类敏感PA(CSPA)在5个病程中出现。在患者7中,在CAZ/AVI输注的第五天观察到头孢他啶最低抑制浓度(MIC)升高(从2μg/mL增加到≥64μg/mL)的CSPA分离株。在患者8中,PA分离株在不同病程中从CRPA变为CSPA。患者1同时感染了碳青霉烯类耐药鲍曼不动杆菌。根据由14个KP和PA组成的敏感性曲线(表2),5个(35.7%)对碳青霉烯类耐药,3个(21.4%)对CAZ不敏感。
2.治疗方案临床反应评估
5例患者因反复感染接受2个疗程的CAZ/AVI给药(患者8为面部蜂窝织炎,患者11为肠粘连,患者15、23和24为BSI),间隔时间分别为44天、4天、15天、24天和21天,在第一个疗程停止后。共评估了30个疗程的CAZ/AVI,均为既往抗GNB抗菌药物失败后的挽救性治疗。碳青霉烯类(40.0%,12/30)、替加环素(40.0%,12/30)、阿米卡星(36.7%,11/30)和多粘菌素B(33.3%,10/30)是CAZ/AVI之前最常用的抗生素处方。10个疗程(33.3%,10/30)个疗程的CAZ/AVI作为GNB单药治疗,20个疗程(66.7%,20/30)疗程与GNB抗生素联合使用,主要是多粘菌素B(45.0%,9/20)、碳青霉烯类(30.0%,6/20)、阿米卡星(20.0%,4/20)和替加环素(20.0%,4/20)。CAZ/AVI治疗的中位持续时间为8.5(5.8,11.5)天。15个(50.0%,15/30)疗程出现临床改善,包括3个单药治疗和12个联合治疗,其中大部分使用多粘菌素B(40.0%,6/15)。绝大多数微生物反应天数在2至4天之间,患者7为18天。
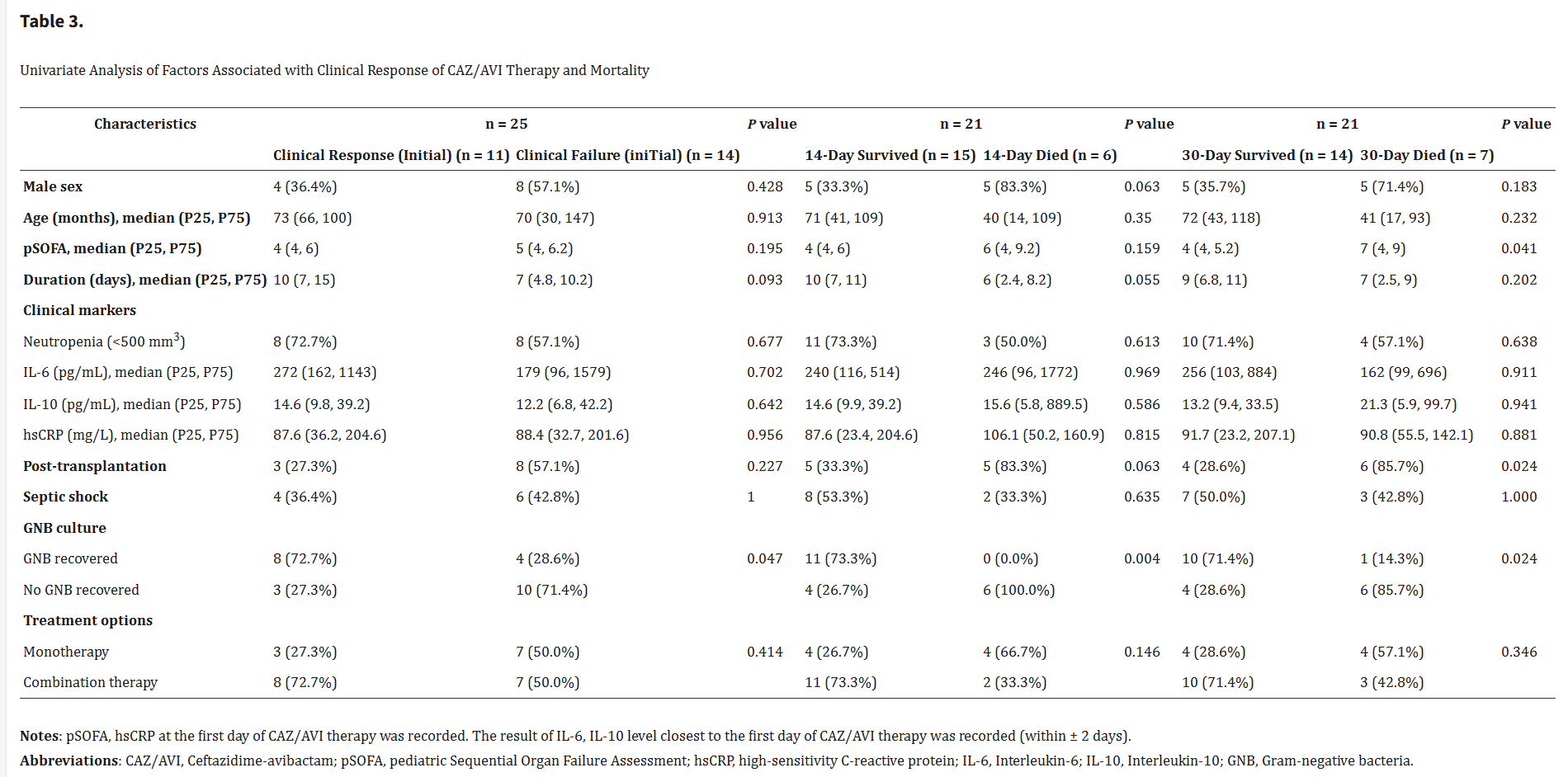
为了探索与临床反应相关的可能因素,分析了25名患者最初25个疗程的数据,以避免个体第二个疗程的数据不独立(表3和4)。与未恢复GNB的组(23.1%,3/13)相比,确诊 GNB 病原体的患者表现出更好的临床反应,为66.7%(8/12) (P = 0.047)。在其他特征上,如年龄、性别、首日pSOFA评分、CAZ/AVI治疗持续时间、中性粒细胞减少症、临床标志物(包括IL-6、IL-10和hsCRP)、基础疾病、原发感染类型、移植、感染性休克或治疗选择(单药治疗或联合治疗))在临床反应结果方面没有发现显著差异。
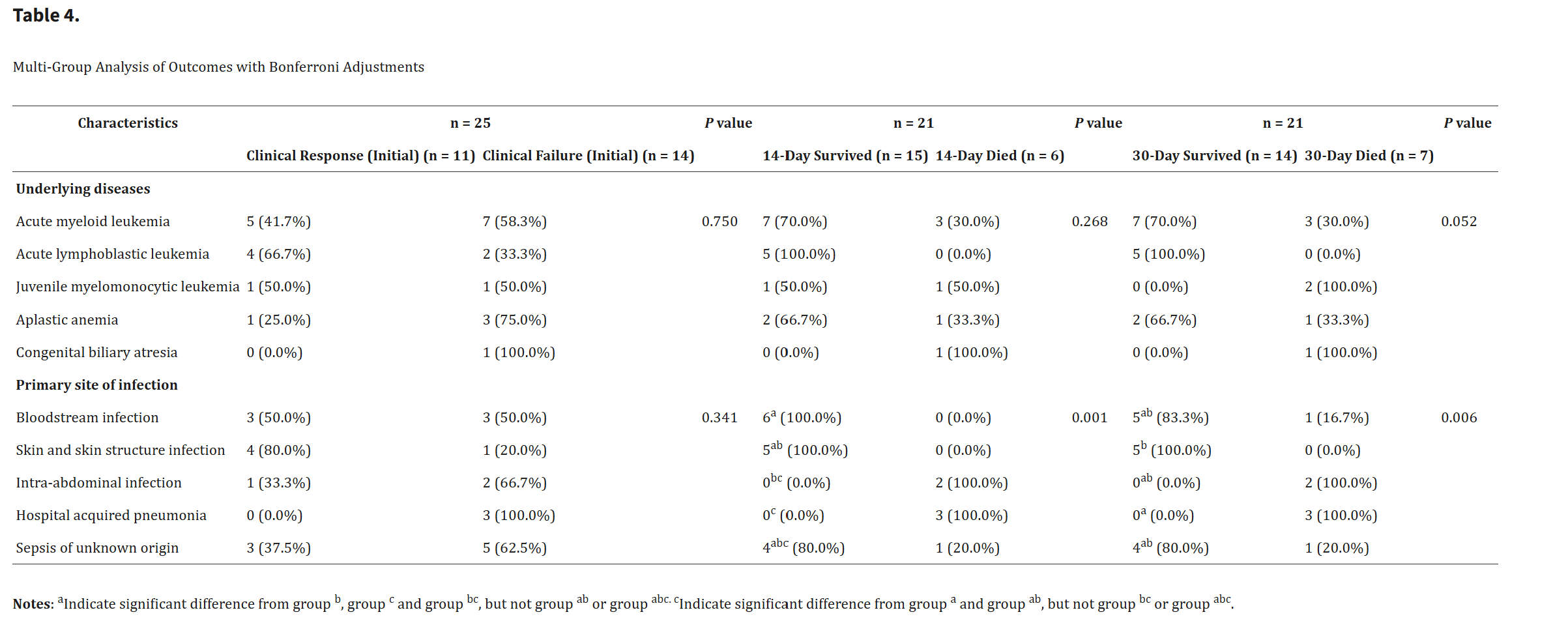
CAZ/AVI治疗开始后14 d、30 d和90 d观察时间点的全因死亡率分别为24.0%(6/25)、28.0%(7/25)和44.0%(11/25)。由于样本量较小,本研究采用单因素分析代替多因素logistic回归来探讨与死亡率相关的因素。14天死亡率与没有确诊的GNB病原体(100% vs 0%,与GNB康复组相比,P=0.004)显着相关(表3),以及以腹腔内感染(IAI)和医院获得性肺炎(HAP)为主要感染部位(100% vs 0%,分别与血流感染(BSI)和皮肤和皮肤结构感染(SSSI)组相比,P = 0.001)(表4)。30天死亡率与没有确诊的GNB病原体(85.7% vs 14.3%,P = 0.024)、CAZ/AVI治疗第一天较高的pSOFA评分(7 vs 4,P=0.041)、移植史(85.7% vs 28.6%,P=0.024)(表3)和HAP作为主要感染部位(100% vs 0%,与SSSI组相比,P=0.001)(表4)。其他特征(如基础疾病、CAZ/AVI持续时间、炎症生物标志物、单一疗法或联合疗法等治疗选择)在组间没有显着差异。
3.病例匹配分析
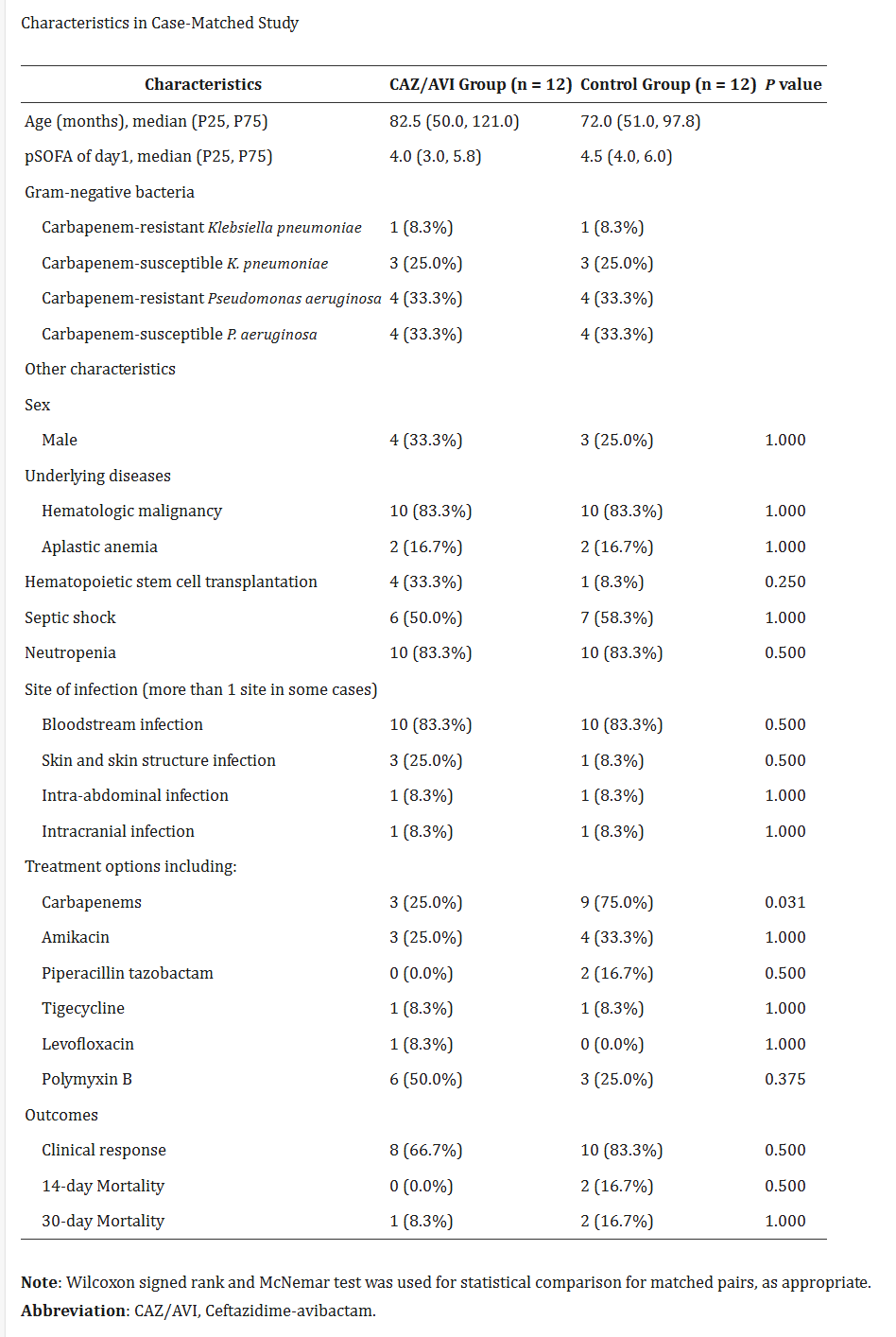
12个病例匹配对的特征和结果如表5和S3所示。对照组的大多数患者接受了含有碳青霉烯类药物的抗生素。包括临床反应、14天死亡率和30天死亡率在内的结局没有显着差异。
五、文章小结
CAZ/AVI可用作GNB康复的免疫抑制儿童的挽救性治疗选择。经过仔细评估,我们提供了CRKP或CRPA相关SSSI的CAZ/AVI治疗的支持性经验。当将CAZ/AVI应用于免疫抑制且GNB未恢复的严重疾病或以HAP为主要感染部位的儿童时,应谨慎。

上一篇:糖尿病加速轻度认知障碍诊断后第一年内阿尔茨海默病进展的研究