发布时间: 2025-05-15 13:27:53
2025年3月18日,在《EClinicalMedicine》上一篇名为“Disproportionality analysis of interstitial lung disease associated with novel antineoplastic agents during breast cancer treatment: a pharmacovigilance study”的研究论文被发表,本研究旨在检测与乳腺癌治疗中使用的新型抗肿瘤药物相关的间质性肺病(ILD)不成比例报告的信号。
一、研究背景
研究表明,一些抗肿瘤药物可能与ILD有关,但缺乏大规模的真实世界数据。本研究旨在检测与乳腺癌治疗中使用的新型抗肿瘤药物相关的ILD不成比例报告的信号。
二、数据来源
我们从2004年1月1日至2023年12月31日的FAERS数据库和2004年1月1日至2024年3月31日的JADER数据库中收集了FDA批准的用于治疗乳腺癌的新型抗肿瘤药物的数据,包括TKI(拉帕替尼、奈拉替尼、图卡替尼)、mAb(曲妥珠单抗、帕妥珠单抗)、ADC(曲妥珠单抗emtansine、曲妥珠单抗deruxtecan、sacituzumab govitecan)、ICI(帕博利珠单抗、atezolizumab、avelumab)、CDK4/6抑制剂(palbociclib、ribociclib、abemaciclib)、PARP抑制剂(olaparib、niraparib、talazoparib)和PI3K/AKT/mTOR抑制剂(alpelisib、依维莫司、capivasertib),我们还考虑了这些药物的商品名称。为确保方法学的透明度和可重复性,本研究遵循READUS-PV指南。
三、研究方法
我们使用报告比值比(ROR)进行了不成比例的分析,以评估新型抗肿瘤药物治疗乳腺癌与ILD发生之间的潜在关联。在确定信号后,我们描述性地分析了病例的临床特征。从治疗开始到ILD事件发生的时间被分析为发作时间(TTO)。我们使用Kruskal-Wallis检验来比较不同药物之间的ILD TTO,使用Wilcoxo秩和检验来比较两个数据库中同一药物的TTO。我们应用单变量logistic回归来评估药物类别(新型抗肿瘤药物与化疗药物)与ILD发展之间的关联。计算每种药物类别的比值比(OR)和相应的95%CI。此外,创建了火山图以直观地比较新型抗肿瘤药物和化疗药物之间的ILD信号。单变量Cox模型评估了每种药物类别对ILD的个体影响,而多变量模型评估了临床特征的影响。我们还对医疗保健专业人员报告的ILD病例进行了不成比例的分析,以进一步验证结果的可靠性。所有统计分析均使用R(版本4.3.1)和RStudio程序进行。
四、主要结果
1、基线特征
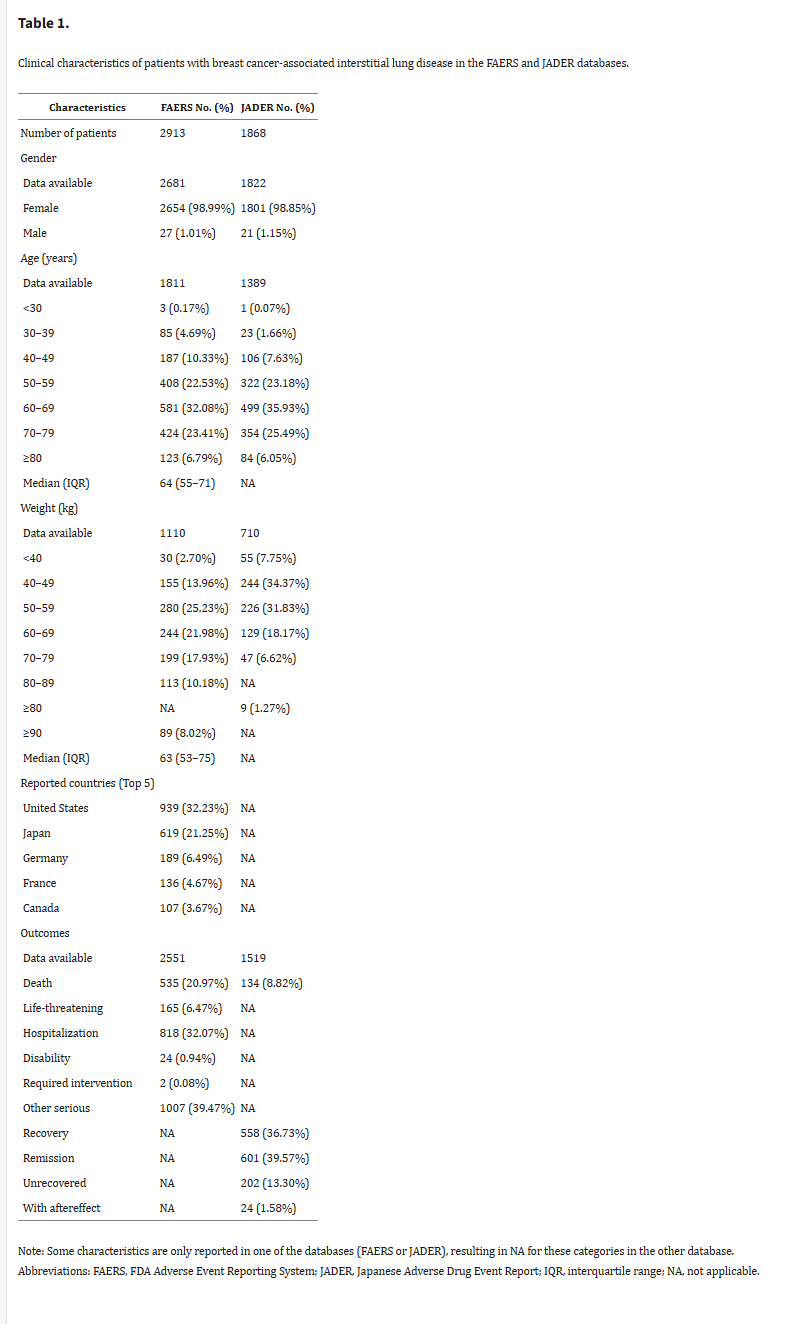
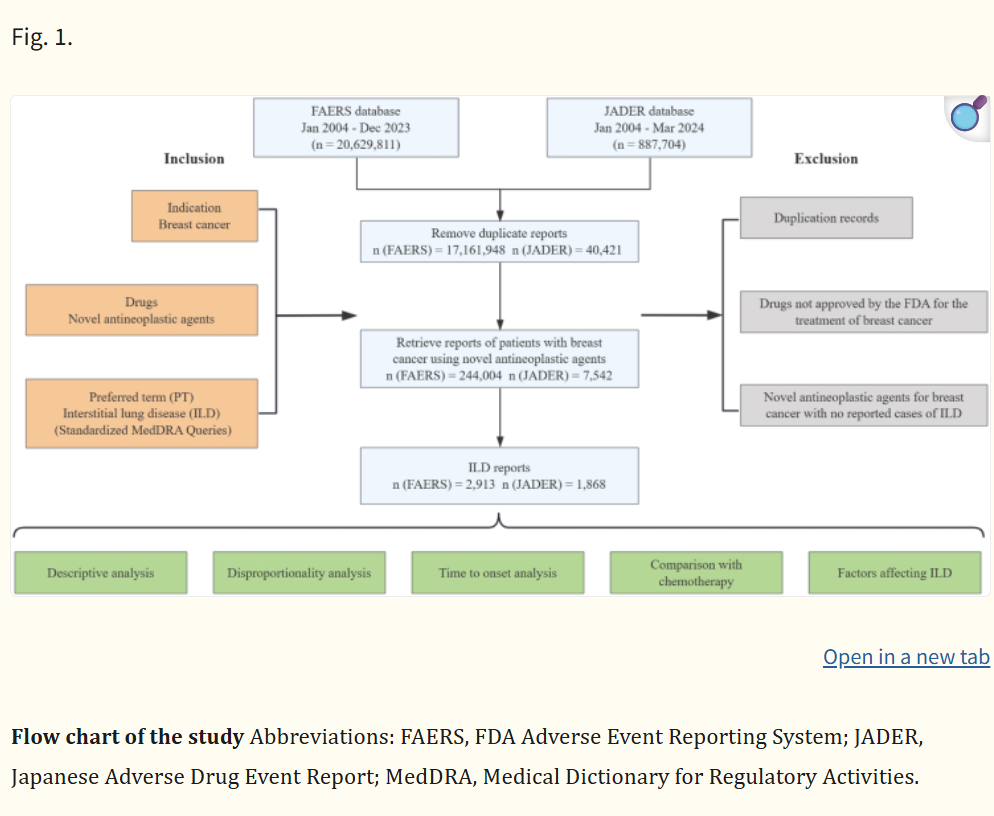
在FAERS中,共确定了2913例ILD病例和3175例报告。中位年龄为64(四分位距[IQR]55-71)。中位体重为63公斤(IQR:53-75)。在2551例有可用结局的病例中,超过一半(67.86%,1731)涉及严重结局,包括死亡(20.97%,535)、危及生命(6.47%,165)、残疾(0.94%,24)和其他严重(39.47%,1007)。同样,我们在JADER中确定了1868例ILD和1894例相关报告。他们中的大多数年龄在60岁以上(67.46%,937/1389),主要在40-59公斤(66.20%,470/710)范围内,8.82%的病例(134/1519)是致命的(表1)。数据处理流程如图1所示。
2、不成比例分析
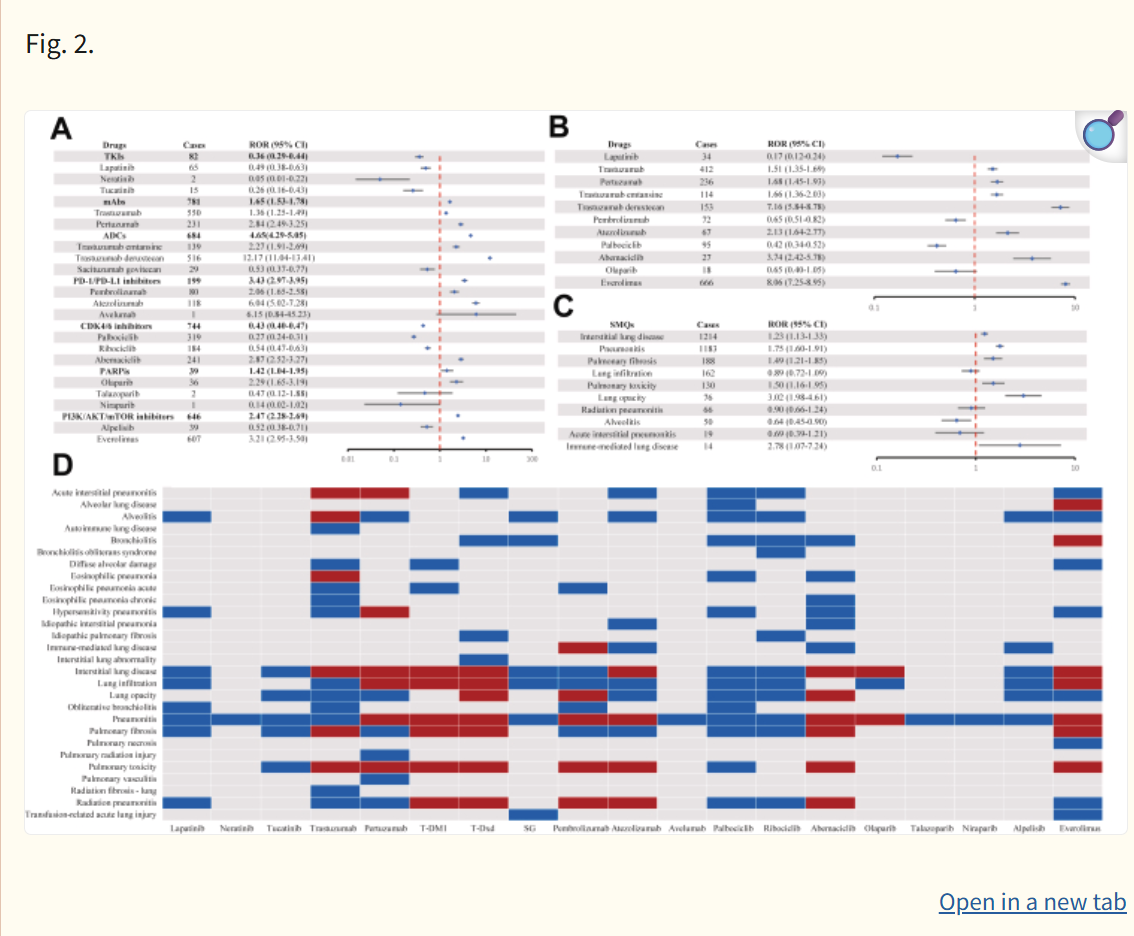
在FAERS中,确定了9种新型抗肿瘤药物作为ILD报告不成比例的信号(图2A):T-Dxd的ROR为12.17、atezolizumab(ROR 6.04)、依维莫司(ROR 3.21)、阿贝西利(ROR 2.87)、帕妥珠单抗(ROR 2.84)、奥拉帕尼(ROR 2.29)、曲妥珠单 emtansine(T-DM1)(ROR 2.2)、帕博利珠单抗(ROR 2.06;95% CI 1.65-2.58) 和曲妥珠单抗(ROR 1.36)。此外,在PT水平,在各种药物中鉴定出49个阳性信号,图2D显示了与新型抗肿瘤药物相关的IL事件的PT。T-Dxd和依维莫司的信号最多,各呈7个。紧随其后的是曲妥珠单抗、帕妥珠单抗、T-DM1和abemaciclib,各有6例。Pembrolizumab报告了5个信号,atezolizumab报告了4个信号,奥拉帕尼报告了2个信号。单变量Cox分析的结果由ROR提供高度一致,ADC(HR 2.83)、ICI(HR 2.17)和PI3K/AKT/mTOR抑制剂(HR 2.84)与其他新型抗肿瘤药物相比,ILD报告几率更高。相比之下,TKI(HR 0.57)和CDK4/6抑制剂(HR 0.34)与ILD报告几率较低相关。在JADER中,7种药物被确定为ILD报告不成比例的信号(图2B):依维莫司(ROR 8.06)、T-Dxd(ROR 7.16)、abemaciclib(ROR 3.74)、atezolizumab(ROR 2.13)、帕妥珠单抗(ROR 1.68)、T-DM1(ROR 1.66)、和曲妥珠单抗(ROR 1.51)。
3、多变量逻辑回归分析
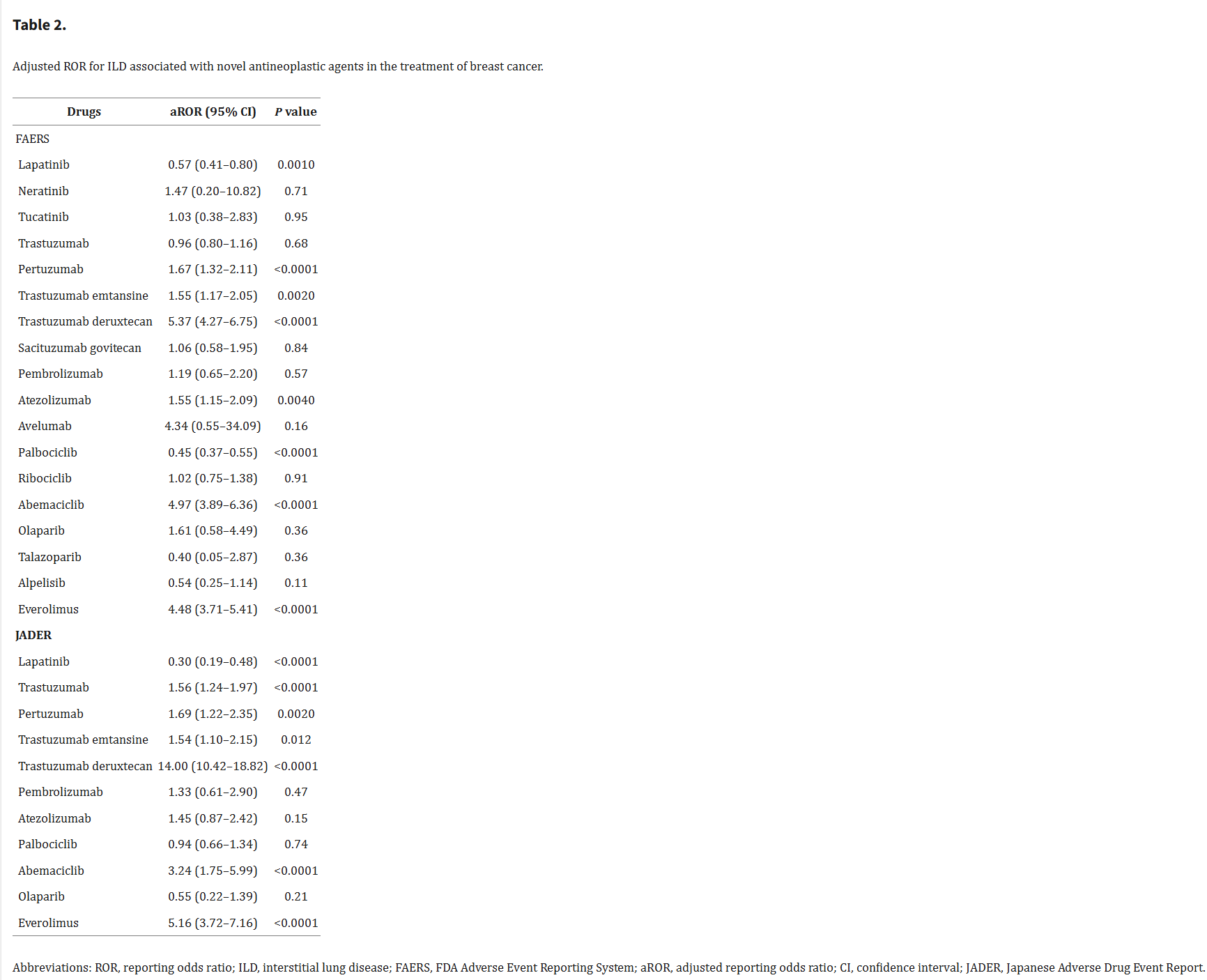
在FAERS中使用多变量logistic回归分析调整混杂因素后,我们确定了6个可能与ILD相关的新型抗肿瘤药物信号:T-Dxd(aROR 5.37)、abemaciclib(aROR 4.97)、依维莫司(aROR 4.48)、帕妥珠单抗(aROR 1.67)、T-DM1(aROR 1.55)、和atezolizumab(aROR 1.55)。同样,在JADER中,确定了6种新型抗肿瘤药物信号:T-Dxd(aROR 14.00)、依维莫司(aROR 5.16)、abemaciclib(aROR 3.249)、帕妥珠单抗(aROR 1.69)、曲妥珠单抗(aROR 1.56)和T-DM1(aROR 1.54)(表2)。值得注意的是,这些因素也在调整前的不成比例性分析中被识别出来,表明调整前后观察到的关联总体一致。
4、ILD的发病时间分析
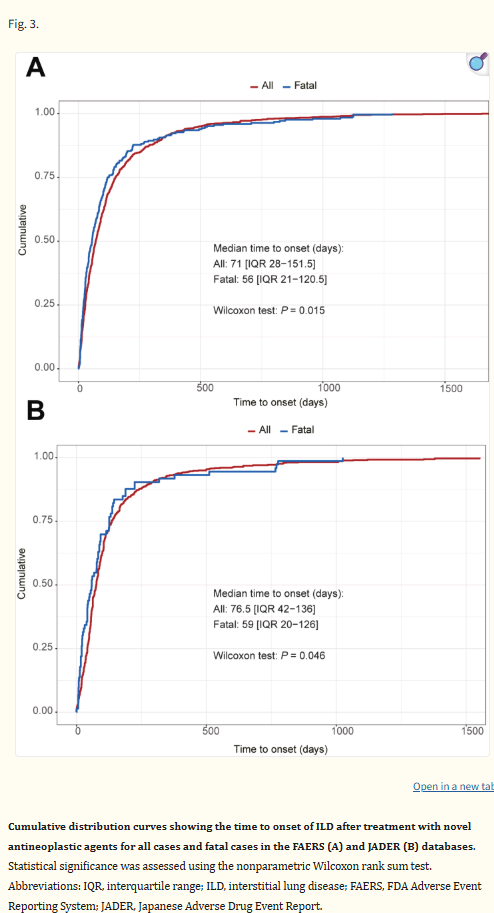
在FAERS中,与所有新型抗肿瘤药物相关ILD中位起效时间为71天(IQR:28-151.5),而致命病例为56天(IQR:21-120.5),差异显著(P = 0.015)(图3A)。在JADER中,中位起效时间为76.5天(IQR 42-136),而致命病例为59天(IQR:20-126),表明存在显著差异(P = 0.046)(图3B)。结果表明,除了abemaciclib(FAERS的中位起效时间:57.5天[IQR:27.8–143]vs.JADER的205天[IQR:89.8–279],P = 0.0032)和依维莫司(FAERS的56天[IQR:23.5–104.5]vs.JADER的61天[IQR:44–104.5],P = 0.017),两个数据库中相同药物的起效时间差异没有统计学意义。
5、死亡病例分析
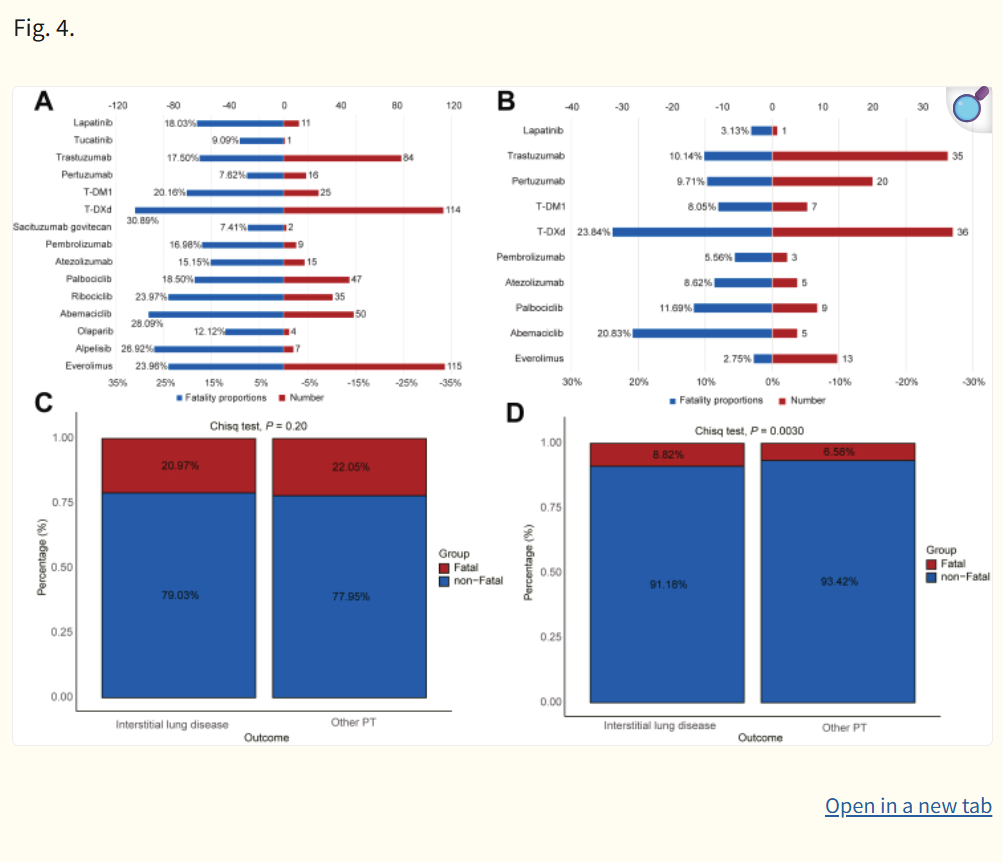
在FAERS中,超过20%的ILD病例有致命的结局。T-Dxd的死亡率最高(30.89%)(图4A)。在JADE中,T-Dxd不仅死亡率最高,为23.84%,而且死亡病例数最高(36/151)(图4B)。在SMQ水平,大多数死亡病例归因于ILD和肺炎,分别占260例(23.55%)和199例(20.49%)。此外,我们在JADER中的分析显示,与没有ILD的组(6.58%,409/6219)相比,ILD组的死亡风险(8.82%,134/1519)显着更高,P = 0.0030(图4D)。然而,在FAERS中没有观察到类似的发现(ILD:20.97%,535/2551与其他PT:22.05%,16269/73783;P = 0.20)(图4C)。
五、文章小结
总之,多种用于乳腺癌的新型抗肿瘤药物,特别是T-DXd、abemaciclib、依维莫司、T-DM1和帕妥珠单抗,显示出与ILD相关的不成比例报告的信号。大多数药物的起效时间在给药后早期出现,致命病例发生得更早。与传统化疗药物相比,新型抗肿瘤药物与ILD的相关性更强。年龄和体重是影响ILD发生的潜在因素。这些发现可以帮助临床医生及时识别和管理ILD,从而提高患者的治疗持久性和生活质量。